בשימוש על ידי נוגדנים מונוקלוניים במילים אחרות, זה אומר חלבונים המיוצרים על ידי קו תאים מאוד ספציפי או שיבוט תאים. המאפיינים הספציפיים שלהם כוללים שיש להם רק קביעת אנטיגנים יחידה. ניתן לייחס את ייצור החומר המשמש לחיסון ללימפוציט B יחיד.
מהו נוגדן מונוקלוני?
ברגע שמתגלה אנטיגן על ידי נוגדן המכוון אליו ויוצר עמו קשר, זה נקרא אפיטופ. בדרך כלל ישנם מבנים מגוונים על נגיף, משטח חיידקי או פתוגן אחר על גבי אפיטופ, כך שאלו מגיבים עם נוגדנים מאוד ספציפיים וגורמים למערכת הגנה באורגניזם. זה יוצר תערובת שלמה של נוגדנים, כולל לימפוציטים מסוג B שונים ליצירת קונוסים, שמופעלים ואז מוכפלים.
לימפוציטים B הם חלק מתאי הדם הלבנים והם לבדם מסוגלים לקשור נוגדנים באורגניזם. מכאן שהם מהווים חלק מהותי ממערכת החיסון. הם נשאים של המידע ליצירת תגובה נגדית, וכאשר הם מופעלים על ידי אנטיגנים אקסוגניים, הם יכולים להפוך לתאי פלזמה, שמייצרים אז נוגדנים מספיקים.
לעומת זאת, נוגדנים מונוקלוניים הם מאוד ספציפיים רק נגד קובע גורם בודד של הפתוגן ולכן מיוצרים מלימפוציט B בטכנולוגיית היברידית. כאן נוצרים נוגדנים מונוקלוניים על ידי היתוך תאים בין לימפוציטים ותאי גידול, לפיהם האחרונים יכולים להתחלק ללא הגבלת זמן. זה בתורו מאפשר את הריבוי ובסופו של דבר היעילות בתרופות ובאנטיביוטיקה אפשרית ברגע שנוגדנים מונוקלוניים אנושיים z. יש להשתמש נגד מחלות זיהומיות. נוגדנים כאלה יעזרו גם באבחון גידולים, לפיהם ניתן לאתר תאים מנווונים באמצעות משטח שונה.
השפעה פרמקולוגית
על מנת לאבחן פתוגנים, יש צורך להגדיר מאפיינים מסוימים של מערכת החיסון. ניתן לראות את אלה על פני השטח. ברגע שאורגניזם משתמש במערכת החיסון שלו בכדי להתחיל בתגובות הגנה, הלימפוציטים מסוג B מונפשים לייצור נוגדנים. זה יוצר אוסף של נוגדנים בעלי תכונות שונות, ואילו החלוקה בהתאמה יוצרת שיבוט של תאי B, שהנוגדנים מגיבים לאנטיגן אפשרי.
תהליך שפותח על ידי זוכי פרס נובל סזאר מילשטיין וז'ורז 'קהלר ופורסם יחד עם נילס ירן בשנת 1975 משמש לייצור נוגדנים מונוקלוניים. באמצעות השיטה המפותחת שלהם ניתן היה לייצר באופן ספציפי סוג מסוים של נוגדן, אשר בתורו אפשר היה לטפח במבחנה, דבר שאינו אפשרי רק בשום כמות, אלא גם עם מאפיינים ספציפיים מאוד של הנוגדנים, שבתורם ניתן להשתמש בהם תרופות מתאימות. התהליך הופך את תאי החיסון לחזקים יותר ויכולים גם לשרוד כתרבות מיושמת. מכיוון שהאיחוי של תאי גידול ותאי חיסון מביא לשיעור גדילה בלתי מוגבל באופן משמעותי, תא זה ידוע כתא היברידיומה.
יישום רפואי ושימוש
ברגע שמתנוונים תאי B בעלי יכולת קבועה לחלק נתיכים עם תאי B היוצרים נוגדנים, נוצרים נוגדנים מונוקלוניים זהים גנטית. היברידומים כאלה הם זהים מבחינה מבנית ומכוונים רק להכיר בתכונה מאוד ספציפית, ומכאן המונח "מונוקלוני".
הייצור בענף התרופות קשה מאוד והמחקר נבדק בעיקר על עכברים. לבעל החיים מוזרק אנטיגנים כדי לעורר חיסון. הלימפוציטים ב B הטחול, המעובדים כתאים ומתמזגים בתאי מיאלומה, הם בעלי עניין מיוחד. האחרונים הם לימפוציטים מנווונים היוצרים גידולים.
אנזים שמכליל חומצה גרעין גורם אז להיווצרות תאים היברידיים. ההתמזגות של תאי הגידול האלמותיים ותאי B בייצור הנוגדנים שלהם מייצרת את הכמות העצומה, שגדלה אז כ מושבות תאים על ידי בחירת שיבוטים שונים של תאים ויוצרים שוב ושוב את אותו הנוגדן. ניתן להשתמש באלה בדיוק לטיפול רפואי, למשל. B. לאבחון מסרטנים וגידולים. נוגדנים מונוקלוניים משמשים כעת גם לטיפול בדחיית השתלות.
אתה יכול למצוא את התרופות שלך כאן
➔ תרופות לחיזוק ההגנה ומערכת החיסוןסיכונים ותופעות לוואי
השימוש בנוגדנים מונוקלוניים הוכח קלינית מזה מספר שנים ומייצג אזור חדש וגדל בהתפתחות התרופות. ב. חיסונים פסיביים הוכיחו את עצמם כיעילים, כגון סרנה נגד ארס נחשים, טטנוס אימונוגלובולין או אנטיוקסין דיגיטלי.
התערובת המורכבת והייצור של נוגדנים כאלה אינה מתרחשת מהדם עצמו, אלא כסינתזה ביולוגית מולקולרית של חלבונים. רק אימונוגלובולין G מתאים למוצרי רפואה, שכן הוא בצורת Y וכך מאפשר התפתחות נוגדנים.
בטיפול בסרטן נוגדנים מונוקלוניים שמטרתם להמיס את התאים המנווונים ובכך לחסום את מסלולי האיתות של גורמי הגדילה, כולל היווצרות כלי דם חדשים. אם הטיפול אינו מגיב, ניתן להסיר את תאי B מדמו של המטופל על ידי עירוי ריטוקסימאב.
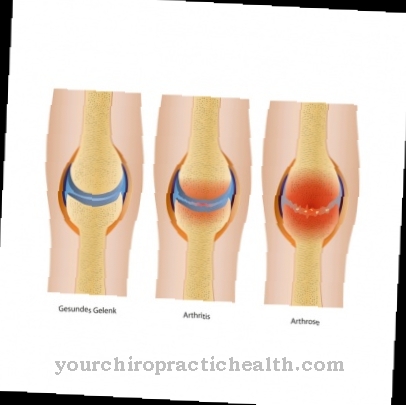
במקרה של מחלות מפרקים, כמו דלקת מפרקים שגרונית, התהליכים הדלקתיים מופעלים ומתעצמים על ידי אנטיגנים, מה שמוביל בסופו של דבר לפירוק רקמות העצם והפרקים. נוגדנים יוצרים שיווי משקל חדש, שמתערבים ספציפית בתהליך הדלקתי.
לבסוף, השימוש בנוגדנים מונוקלוניים משמש גם באבחון מיקרוביולוגי. ניתן לזהות ולזהות זיהומים טפיליים, חיידקיים או נגיפיים בצורה טובה יותר, מכיוון שהפתוגנים יכולים לזהות אותם.
רכיבים פעילים רקומביננטיים מאושרים לטיפול רק אם הטיפול בעבר לא הצליח והופכים הכרחיים לשינוי מחלות. קיים סיכון שהטיפול יכול להוביל למספר מוגבר של זיהומים חדשים. הסיבה לכך היא שאמנם נוגדנים מונוקלוניים מכירים במבני חלבון ספציפיים על ידי חיקתם, אך הם עצמם נשארים חלבונים המועברים רק על ידי עירוי או הזרקה על ידי הרופא. תגובות שמתרחשות הן תופעות לוואי באתר ההזרקה, כגון: ב. תגובות או אלרגיות בעור.


.jpg)
.jpg)

.jpg)











.jpg)