אחד האלמנטים הנפוצים ביותר בכדור הארץ הוא חַמצָן. כחמישית נפח של יסוד כימי זה קיים באוויר, אם כי הוא חסר צבע, חסר טעם ונטול ריח. הוא נמצא גם באותה תדירות במים ובקרום כדור הארץ. רוב היצורים החיים והתאים החיים זקוקים לחמצן לנשימה.
מה זה חמצן
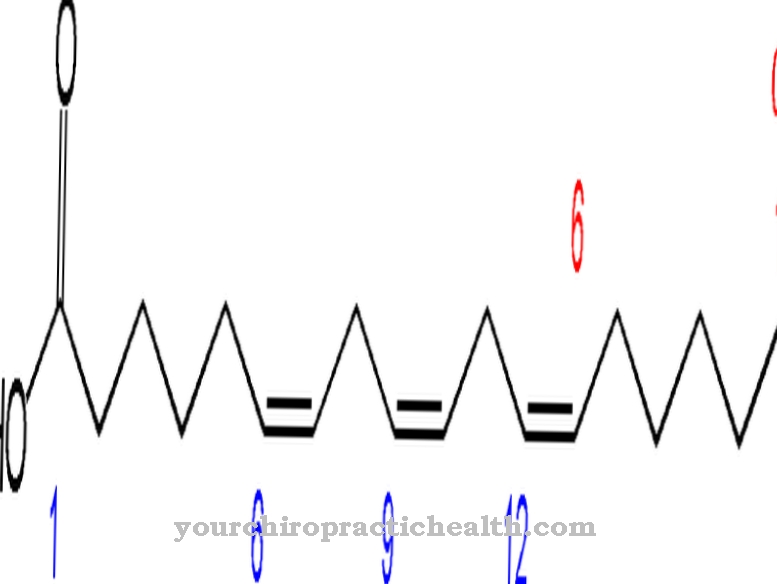
בטבלה המחזורית, חמצן מסומן בסמל "O" ויש לו את המספר האטומי "8." רוב הזמן הוא מתרחש בתרכובות וכמולקולה של שניים ושלוש אטומים. האחרון ידוע גם בשם "אוזון".
סלעים ומינרלים מכילים לרוב חמצן, כמו למשל B. קוורץ, שיש או אבן גיר. לעומת זאת, אטומי חמצן חופשיים ואינדיבידואליים מתאפשרים בצורה יציבה בתנאים קיצוניים. זה המצב בוואקום של החלל. ניתן להפריד את החמצן מהאוויר על ידי זיקוק ואז, כשהוא נוזל, מקבל צבע כחלחל. משתמשים בתנאים כאלה למשל ב. בשכלול מתכות, מיצוי כימיקלים או כאפליקציה רפואית לתמיכה בחיים.
חמצן תמיד גזי בתנאים רגילים ובשילוב עם אלמנטים אחרים מעורב בתהליכי בעירה רבים. הוא התגלה ונחקר בשנת 1772 על ידי הכימאי והרוקח קרל וילהלם שייל.
חמצן מבודד זה כגז, תהליך שהיה דומה לתהליך הפיסטור, ובדרך זו גילה גם יסודות אחרים, למשל. B. חנקן. עם זאת, מכיוון שהוא לא פרסם את עבודותיו על כך רק לאחר מספר שנים לאחר מכן, הכימאי ג'וספ פריסטלי הגיע לפניו, אשר, באופן עצמאי, גילה את אותה תגלית, כולל השפעות החמצן על תהליכי הבעירה, אף כי התהליך עצמו היה עדיין שם לא פוענח.
בעבר, האש נתפסה בצורה מטאפיזית יותר, כאחד מארבעת היסודות שהרכיבו. בנוסף לאש, היו אדמה, אוויר ומים. במאה ה -17, אז שילב חום באש, וכשנתגלה במאה ה -18 החומר הפך ליסוד. אך רק באמצעות המלומד הפרטי אנטואן לורן דה לבואה, ניתן היה אז לפרש נכון בעירה ונשימה. הוא ביצע ניסויים בחמצן טהור וקבע את הרכב האוויר.
פונקציה, אפקט ומשימות
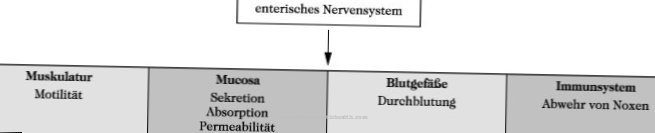
באטמוספרה, חמצן נמצא תמיד בגזים ומומס במים. האלמנט מאוד תגובתי ומיוצר בעיקר על ידי צמחים באמצעות פוטוסינתזה ונצרך שוב באמצעות נשימה ותהליכי בעירה אחרים. אצות כחולות-ירוקות וציאנו-בקטריות ממלאות גם הן תפקיד בתהליכים אלה, שהחלו לפני יותר משלושה מיליארד שנה לאגור אור שמש ולהשתמש בהן לסינתזה של תרכובות אורגניות. חמצן היה ולכן הוא מוצר פסולת יעיל מאוד.
בני אדם, צמחים וחיידקים זקוקים לחמצן כדי להיות מסוגלים לחיות ולייצר אנרגיה בצורה זו. העיבוד מתרחש במיטוכונדריה, לפיו החמצן בשרשרת הנשימה הופך להיות שוב למים. בתורו אנזימים מפרקים חומרים באורגניזם באמצעות חמצן.
חינוך, התרחשות, תכונות וערכים מיטביים
התגובה הטובה של החמצן ותרכובותיו עלולה להוביל גם להרס מסוכן יותר של מבני התא. למרות שבני אדם זקוקים לחמצן כדי לנשום, יותר מדי חמצן הוא רעיל, ובכמויות גדולות, אפילו יכול להוביל לנזק לריאות לאורך תקופה ארוכה.
האורגניזם האנושי מתפקד עם ריכוז חמצן בסביבות 21 אחוז באוויר. תאי דם אדומים נושאים חמצן מהריאות לאיברים. אם זה גבוה מדי, האלובולים מתנפחים ותאי הדופן שבריאות הופכים לנמק, הפנאומוציטים נפגעים והמוני חלבון מופקדים על הדופן הפנימית. התוצאה היא חילופי גז מופחתים מאוד בנשימה ובזרם הדם.
באופן דומה, תערובת גז עם חמצן מוגבר עלולה לפגוע במערכת העצבים המרכזית ולגרום לתסמיני עצבים מרכזיים. אנו מדברים על אפקט פול ברט אשר יכול להתבטא ברעשי אוזניים, סחרחורות, בחילות, הקאות, אך גם במצבים דרסטיים כמו שינויי אישיות ובלבול נפשי. זוהי תופעת לוואי נפוצה, בעיקר בצלילה, כך שיש להקפיד על תכולת החמצן ועומק הצלילה המרבי.
מחלות והפרעות
לרוב האורגניזמים אנזימים מגנים כמו פרוקסידאז וקטליז לניקוי רעלים מהחמצן. פירוק החמצן בגוף יוצר רדיקלים חופשיים הפוגעים ב- DNA המיטוכונדריאלי וניתן לסתור אותם על ידי נוגדי חמצון. כאלה נבלעים במזון והם z. B. ויטמינים C, A ו- E, מינרלים ויסודות קורט.
חוסר איזון בין צמצום וחומרים מחמצנים בתאים מביא לשיבוש בתפקוד הגמילה של הגוף עצמו ופוגע בתא. זה מכונה לחץ חמצוני, אשר בתורו מוביל לתהליכי הזדקנות.
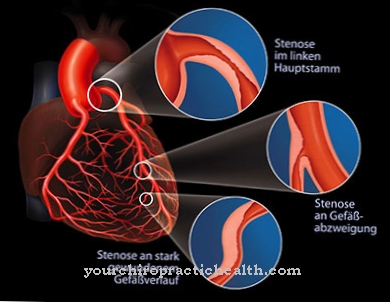
מחסור בחמצן נפוץ במחלות לב וריאות. זה בתורו משפיע על העורקים והרקמות של כל האיברים החיוניים. כאן יש לתת חמצן ולספק גם הנשמה מלאכותית. החמצן משרת גם את תהליך ריפוי הפצע עצמו. פצעים יכולים להידבק לאחר הניתוח, בו מתח החמצן ברקמה ובתאי החיסון בדם ממלא תפקיד שמשתמש ברדיקלים חופשיים כדי להילחם בחיידקים בגוף. ברוב המקרים, חמצן מסופק גם לאחר ההרדמה על מנת להפחית את הסיכון לזיהום.
מחלות הקשורות למחסור בחמצן כרוני דורשות טיפול חמצן ארוך טווח. הסיבות יכולות להיות צמצום דרכי הנשימה, תסחיף ריאתי, פגיעה ברקמת הריאה או מומי לב חמורים.








.jpg)
.jpg)