ה תסמונת ג'וברט מאופיין במומים מולדים של גזע המוח וכן באנדנזה (מום עיכובי, חוסר התקשרות, למשל מוטות מוח, נספח). היפופלזיה (התפתחות תת-עורית) של התולעת המוחית יכולה להתקיים גם היא. חולים הסובלים ממום גנטי רצסיבי אוטוסומלי זה מראים, בין היתר, על התנהגות נשימה ואטקסיה חריגה.
מה זה תסמונת ג'וברט?

© סשקין - stock.adobe.com
אנשים עם תסמונת ג'וברט סובלים מהפרעות התפתחותיות של מערכת העצבים המרכזית ומההפרעות התפקודיות הנובעות מכך. מחקרים רפואיים מעוררים מחלוקת בשאלה האם יש לסווג הפרעה גנטית זו כמחלה בפני עצמה.
לחולים שנפגעו יש מגוון של תסמינים שונים. בגלל זה, אבחנה סופית קשה. ה- JB מאופיין בהטרוגניות של לוקוס גנים נרחב. עד כה זוהו מוטציות גנים מרובות. ניתוח מוטציה הוא נרחב מאוד.
סיבות
תסמונת ג'וברט שייכת לקבוצת הצליופטיות הראשונית. עם הפרעה גנטית זו של cilia הראשוני או של הגוף הבסיסי, יכולים להופיע סוגים שונים של הפרעות התפתחותיות. כתהליכים תאיים מיוחדים, cilia מבצעים משימות שונות. הם פועלים כחיישני כימו, מכאנו ואוסמוזה ומעורבים במסלולי איתות רבים. יתר על כן, הם מבטיחים התפתחות תקינה של איברים.
הם שומרים על הומאוסטזיס של הרקמה של התהליכים ההתפתחותיים הבסיסיים. חלק גדול מהחלבונים המעורבים יוצרים רשת מורכבת באמצעות אינטראקציה. אם איברים אחרים מושפעים בנוסף לתסמינים העיקריים, אז קיימת הפרעה ב- JSRD (תסמונת ג'וברט). מחלה משנית זו מאופיינת בביטויים נוספים של האיברים המערבים את הכליות, הכבד והעיניים.
זוהי תסמונת הטרוגנית גנטית. רופאים מצאו מומים בגן NPHP6 / CEP290 (המקודד ל nefrocystine-6) או בגן NPHP8 / RPGRIP1L (המקודד ל nephrocystine-8). מוטציות גנים אחרות הן MKS3, ARL13B, AHI1, CC2DA2, TMEM216 ו- INPP5E. רק מעטים מהחולים סובלים ממוטציות ב- NPHP4 וב- NPHP1.
תסמינים, מחלות וסימנים
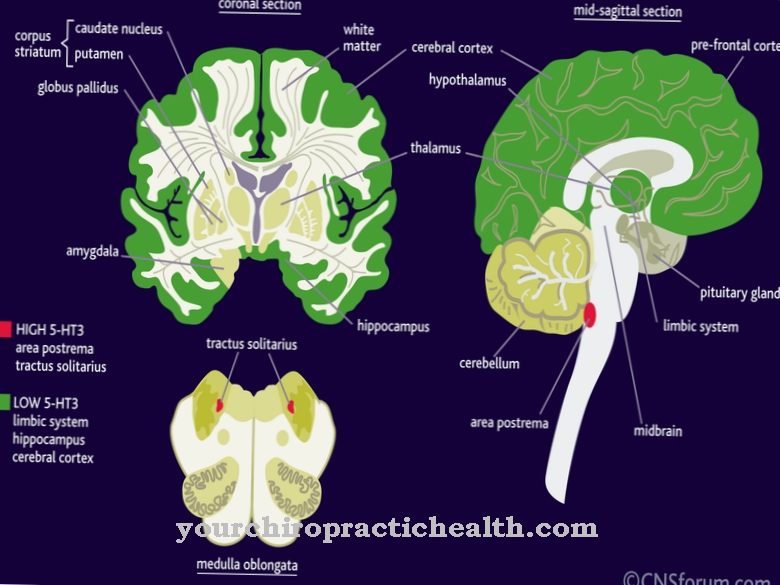
התכונה הפתוגונומונית היא "סימן השיניים הטוחנות" (MTS), שניתן לקבוע באמצעות "הדמיית תהודה מגנטית במוח משוקלל T1". תכונה זו מאופיינת על ידי אגנזה או היפופלזיה של תולעת המוח הקטן או התולעת המוח הקטן. יתר על כן, הפוסה האחורית האחורית (בור בין רגלי המוח) נשאבת פנימה חזק וגבעולי המוח הינם בעלי צורה עליונה בולטת בגלל מום במוח האמצעי.
בנוסף ל- MTS, לעתים קרובות החולים סובלים מהפרעות נשימה, אטקסיה, יתר לחץ דם בשרירים ופיגור פסיכומוטורי. 8 עד 19 אחוז מהנפגעים מראים polydactyly postaxial (ריבוי אצבעות) ושישה אחוזים אנצפלוקלה occitital (meningo), שבו גב המוח מתפיח.
עיוות זה נרשם לראשונה בשנת 1969. השכיחות היא בערך 1: 100,000, יחס שמראה עד כמה לעיתים נדירות מופיעה המחלה. רק מאה מקרים תועדו מאז הסקר הרפואי הראשון. מכיוון שמום גנטי זה מתרחש בצורות שונות ובוואריאנטים שונים, הרופאים מניחים שינויים מרובים בגנטיקה.
אנומליה מדויקת טרם אומתה באופן סופי. עם זאת, מוטציה של הכרומוזום X נחשבת לוודאית. הפרעה זו מועברת על בסיס ירושה רצסיבית אוטוסומלית. מעורבים בו vermis cerebelli (cerebellum, תולעת cerebellar), נזק לרשתית ועין אירוס בולטת.
תסמינים ותלונות המופיעים לעתים קרובות במהלך התקופה של הילודים הם ניסטגמוס ודפוס נשימה לא סדיר כתופיפיה ואפנומיה אפיזודית. ילדים צעירים יכולים לפתח היפוטוניה. עם הגיל המתקדם מתפתחים חוסר איזון והליכה לא אחידה (אטקסיה). תסמינים עיקריים אלה מכונים גם אבני דרך מוטוריות.
המטופלים הם בעלי רמות שונות של יכולות קוגניטיביות ויכולים להיפגע בצורה קשה, אך הם גם יכולים להראות רמת אינטליגנציה תקינה. אברקסיה אוקולו-מוטורית (הפרעת תנועה) אפשרית גם היא.
המאפיינים פגם גנטי זה הם מומים גולגולתיים כמו ראש גדול, גבות מעוגלות וגבוהות, מצח בולט (בולט), פה מעוות, לשון נעה ובולטת בקצב, ואוזניים עמוקות. תסמינים מזדמנים הם nefrophthisis, ניוון רשתית, ו polydactyly.
אבחון ומסלול של מחלה
אבחנה מתבצעת על בסיס אבני הדרך האופייניות שצוינו בעבר של אטקסיה, יתר לחץ דם, אברקסיה oculomotor, ורמיס סרבלי פתוח לאחר השבוע ה -18 להריון ואיחור בהתפתחות. בנוסף, ממצא נוירורדיולוגי אופייני נעשה ב- MRI, ה- MTS (סימן שיניים טוחנות).
תכונה זו, המכונה הסימן הטוחני, נובעת ממומים של המשקעים והמוח האמצעי וכן מההיפופלזיה של תולעת המוח הקטנה. אבחנות דיפרנציאליות נעשות על בסיס מחלות הקשורות באופן הדוק ל- JS כמו JSRD (הפרעה הקשורה לתסמונת ג'וברט), מום דנדי-ווקר (תולעת מוח מוחית לא מבוצעת ללא MTS), סוגים 1 ו -2 של אפרסקיה oculomotor, hypoplasia ponto-cerebral ואטרופיה, 3-c תסמונת, תסמונות אורופציו-דיגיטליות II ו- III וכן תסמונת מקל-גרובר.
שלב I כולל את "ניתוח הפאנלים המבוסס על רצף-הדור הבא" של הגנים JBTS5 (53 אקסון קידוד), JBTS3 (26 אקסונים קידוד), JBTS6 (28 אקסונים קידוד) ו- JBTS9 (36 אקסון קידוד). הגן JBTS4 נבדק לצורך מחיקה הומוזיגוזית על ידי PCR מרובי. בשלב II מנותחים את גני ה- JB האחרים על ידי PCR (תהליך המשכפל רצפי גנים בשרשרת ה- DNA בהתאם לאנזים) ורצף הסנגר לאחר מכן, בהתאם לתכונות הפנוטיפיות, התואמות לירידה בתדרי המוטציה.
על מנת לשלול חוסר איזון כרומוזומלי, ניתוח מערך SNP האבחנתי מבוצע. אם קיימת אישיות נפוצה או אם ידועים כמה אנשים חולים במשפחה, הרופאים מבצעים את בדיקת ההומוזיגוזיות באמצעות ניתוח צימוד בסמן המיקרו-אטליטי שמצדד את הגן וניתוח גנים לאחר מכן באמצעות רצף סנגר. שניים עד עשרה מיליליטר דם EDTA נלקחים מילדים כחומר אבחנתי; מבוגרים הכמות היא חמישה עד עשרה מיליליטר.
גם DNA או חומר רקמות מתאימים. שלב I: חומר DNA גנומי נבדק לצורך קיום של כפילויות או מחיקות באמצעות ניתוח כמותי של הגן NPHP1 באמצעות MLPA. כמויות קטנות מאוד של DNA בגנום נבדקות לצורך מחיקות ושכפול של אקסונים בודדים (קטעי גנים). שלב II: האקסונים המקודדים של הגנים שזוהו עד כה נבדקים באמצעות תדרי הדור הבא. אתרי הריכוז מועשרים בהכלאה של בדיקות.
סיבוכים
תסמונת ג'וברט גורמת לרוב החולים לסבול ממחלות שונות. זה בדרך כלל מוביל לקומה קצרה, הפרעות נשימה, ויתרה מכך - פיגור. ניתן להגביל את ההתפתחות הנפשית של הילד. קשיי הנשימה יכולים להוביל גם לקוצר נשימה, אשר בהחלט יש לטפל בו.
אין זה נדיר כי הוריו של האדם סובלים מדיכאון קשה או מהפרעות פסיכולוגיות אחרות. החולים מראים גם הפרעות באיזון ולעיתים קרובות סובלים מניידות מוגבלת. זה לא נדיר אי נוחות בעיניים ובאוזניים, מה שמוביל לאובדן שמיעה או בעיות ראייה. איכות חייו של המטופל מופחתת משמעותית על ידי תסמונת ג'וברט.
בעזרת טיפולים שונים ניתן להגביל ולטפל בתסמונת ג'וברט. לרוע המזל, לא ניתן לבצע טיפול סיבתי. במקרי חירום ניתן לבצע אוורור חירום גם אם יש מחסור בנשימה. אין סיבוכים מיוחדים בטיפול עצמו. באופן כללי, לא ניתן לחזות אם תוחלת חייו של המטופל תקטן על ידי תסמונת ג'וברט.
מתי כדאי לך ללכת לרופא?
על אם מצפה לקחת חלק בכל הבדיקות הזמינות במהלך ההיריון. בבדיקות נבדק מצב בריאותה של האישה ההרה כמו גם מצב הילדה שטרם נולד. מכיוון שניתן לאבחן תסמונת ג'וברט כבר בשבוע ה -18 להריון, רצוי לעשות שימוש בבדיקות הרפואיות המונעות המומלצות על ידי חברות ביטוח הבריאות. בנוסף, אם יש פגם גנטי בהיסטוריה של אבות ההורים, בדרך כלל מומלץ לייעץ ולבדיקה.
במקרה שלא סביר שלא נמצאה אי סדירות ברחם, בדיקות אוטומטיות של רופאי נשים ורופאי ילדים מתרחשות מיד לאחר הלידה. ניתן לאתר הפרעות נשימה במהלך בדיקות אלו. אם הוריו של הילד מבחינים באי-סדרים חריגים שלפני כן לא התגלו, יש לדון בתצפיות עם רופא. אם יש מוזרויות פיזיות, קומה או עיוותים קצרים, יש לפנות לרופא.
אם בהשוואה ישירה עם ילדים באותו גיל מורגשים בעיות שפה או התפתחות נפשית, יש לפנות לרופא. בירור הכרחי לצורך בירור הגורם. ככל שמתקבלת אבחון מוקדם יותר, ניתן להתחיל טיפולים ממוקדים קודמים לתמיכה בילד. לפיכך יש להתייעץ עם רופא בסימן הראשון לחריגות.
טיפול וטיפול
ההורים זכאים לייעוץ גנטי. אפשרויות הטיפול מגוונות כמו הגורמים למחלה זו. במקרה של הפרעות בהתפתחות מוטורית ויתר לחץ דם, נכנסות לפעולה תוכניות תמיכה חינוכיות, שפה, ריפוי בעיסוק ועשויות להשפיע לטובה על מהלך המחלה.
לאנשים הסובלים מדפוסי נשימה לא תקינים ניתן לקבל החלפת חמצן או אוורור. לחולים עם תסמינים קלים יש פרוגנוזה חיובית. על ידי מרכז הפניה מומחה, יש לטפל בחולים שנפגעו קשה.
תחזית ותחזית
הפרוגנוזה לתסמונת ג'וברט היא לקויה. תסמונת זו הינה הפרעה גנטית. עם הדרישות הרפואיות, המדעיות והמשפטיות הנוכחיות, לא ניתן לרפא זאת. חוקרים ורופאים אסור על פי חוק לשנות את התנאים הגנטיים של אדם באמצעות התערבויות. מסיבה זו הטיפול מכוון לשימוש בטיפולים שנועדו לשפר את איכות החיים הקיימת. ללא שימוש בטיפול רפואי, רווחתו המופחתת של המטופל מצטמצמת עוד יותר.
ככל שניתן לאבחן ולטפל בתסמונת מוקדם יותר, כך התוצאות יהיו טובות יותר. במצבי חירום מצוין אוורור חירום של האדם הנוגע בדבר, אחרת המטופל עלול למות בטרם עת. למרות שטיפולים רבים מורכבים ומיישמים בתוכנית טיפול פרטנית, המחלה הקיימת יכולה להוביל להפרעות משניות. אלה מחמירים את הפרוגנוזה הכללית.
הפרעות תפקודיות קיימות או מגבלות אחרות על התנועה עלולות להוביל למחלות נפשיות. אצל אנשים רבים מתועדים דיכאון זמני או מתמשך, שינויים במצב הרוח או שינויים באישיות. זה מייצג נטל נוסף על האדם הנוגע בדבר ובסביבה, את חיי היומיום של מטופל עם תסמונת ג'וברט לרוב ניתן לנהל רק בעזרת עזרה ותמיכה מספקת מקרובי משפחה. הפרעות באיזון והאטקסיה מחמירות עם הגיל.
מְנִיעָה
מכיוון שטרם נקבע גורם סופי גנטי מדויק, אין אמצעי מניעה במובן הקליני. הדרך היחידה להתמודד עם מומים באורגניזם האנושי היא לנהל אורח חיים בריא.
טִפּוּל עוֹקֵב
ברוב המקרים, למטופל עם תסמונת ג'וברט אין אפשרויות מעקב ישירות או מיוחדות זמינות, כך שהאדם שנפגע תלוי בעיקר באבחון מהיר ובעיקר, מוקדם, של המחלה. ככל שמוכרת המחלה מוקדם יותר, כך בדרך כלל המשך יהיה טוב יותר. לכן מומלץ לפנות לרופא בתסמינים והסימנים הראשונים.
עם מחלה זו, האדם שנפגע תלוי בדרך כלל בטיפול נמרץ ובטיפול שיכולים להקל על התסמינים. גם עזרתם ותמיכתם של הורים וקרובי משפחה קרובים מאוד מבוקשים על מנת לאפשר לאדם שנפגע לנהל חיים תקינים ככל האפשר. לעתים קרובות ניתן לבצע את התרגילים מפיזיותרפיה או פיזיותרפיה בביתך שלך, מה שיכול להקל על הסימפטומים.
לא תמיד ניתן להקל על התסמינים. קשר עם הסובלים מתסמונת ג'וברט יכול גם להיות שימושי מאוד, מכיוון שלא נדיר להחליף מידע. ככלל, תוחלת החיים של האדם שנפגע אינה מופחתת על ידי מחלה זו.
אתה יכול לעשות זאת בעצמך
תסמונת ג'וברט חשוכת מרפא ועזרה יומיומית קשה גם היא. התסמינים של המחלה המולד הם ברוב המקרים בלתי נמנעים. עדיין, יתכן שחלקם יקלו.
מכיוון שהנשימה מופרעת במיוחד בקרב הנפגעים, זוהי נקודת התחלה. אקלים אופטימלי בחדר יכול להועיל. אוויר חימום יבש יכול להחמיר את בעיות הנשימה. לאוויר קר מדי יש השפעה זהה. באופן אידיאלי, טמפרטורת החדר היא סביב 20 מעלות צלזיוס והלחות סביב 50 אחוז. צמחים מקומיים בפרט יכולים לתרום לאקלים מקורה אופטימלי. לחלופין, ניתן להניח בחדר גם מגבות לחות כדי לשמור על הלחות ברמה הרצויה. ניתן לעקוב אחר האקלים המקורה באמצעות מדדי לחות. נקודת פתיחה נוספת המכוונת גם היא לנשימה היא תרגילי נשימה. שימוש קבוע משפר את תפיסת התהליך האוטומטי שאחרת. באופן זה תוכלו למנוע נשימה מהר מדי ולהפסיק נשימה.
זה גם הגיוני אם מי שנפגע לא ישן לבד בחדר. קרובי משפחה עשויים להבחין בהפסקות בנשימה בזמן השינה ולהעיר את המטופל או לעורר אותו לנשום. אבל זו רק אמצעי זהירות.



.jpg)





.jpg)



.jpg)



.jpg)