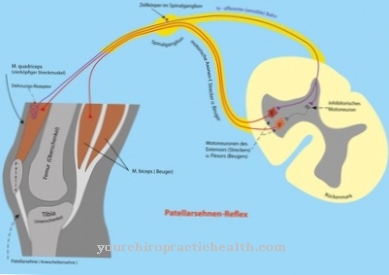
ה פוטנציאל פוסט-סינפטי מרגש הוא פוטנציאל מרגש בקרום הפוסט-סינפטי של נוירונים. הפוטנציאלים האישיים מסוכמים במרחב ובזמן ובכך יכולים ליצור פוטנציאל פעולה. הפרעות הולכה כמו מיאסטניה גרוויס או מיאסטניה אחרות משבשות תהליכים אלה.
מה הפוטנציאל המעורר פוסט-סינפטי?

נוירונים מופרדים זה מזה על ידי פער של 20 עד 30 ננומטר, המכונה גם פער סינפטי. זהו הפער המינימלי בין אזור הממברנה הפרה-סינפטית של נוירון לבין אזור הממברנה הפוסט-סינפטית של תא העצב במורד הזרם.
נוירונים משדרים עירור. לכן, הפער הסינפטי שלהם מגושר על ידי שחרורם של חומרים מסרים ביוכימיים, הידועים גם כמעבירים עצביים. זה יוצר פוטנציאל פוסט-סינפטי מעורר באזור הממברנה של התא במורד הזרם. זהו שינוי מוגבל מקומי בפוטנציאל הממברנה הפוסט-סינפטית. שינוי הדרגתי זה בפוטנציאל מעורר פוטנציאל פעולה באלמנט הפוסט-סינפטי. הפוטנציאל הפוסט-סינפטי המעורר הוא חלק מהולכת העירור העצבית ומתעורר כאשר ממברנת התא במורד הזרם מפולחת.
הפוטנציאלים הפוסט-סינפטיים המרגשים מתקבלים ומעובדים על ידי הנוירון הבא על ידי הוספת מרחבית וגם זמנית. כאשר חורג מפוטנציאל הסף של התא, פוטנציאל פעולה חדש שנוצר מועבר על ידי האקסון.
ההפך מהפוטנציאל הפוסט-סינפטי המעורר הוא הפוטנציאל הפוסט-סינפטי המעכב. זה מוביל להיפרפולריזציה על הממברנה הפוסט-סינפטית, המונעת הפעלת פוטנציאל פעולה.
פונקציה ומשימה
הפוטנציאל הפוסט-סינפטי המרגש והפוטנציאל הפוסט-סינפטי המעכב משפיעים על כל תאי העצב. כאשר חורג מהפוטנציאל לסף שלהם, תאי העצב מקפחים את עצמם. הם מגיבים לקיטוב זה על ידי שחרור משדרים עצביים מעוררים. כמות מסוימת של חומרים אלה מפעילה את תעלות היונים הרגישות למשדר בנוירון. תעלות אלה חדירות ליוני אשלגן ונתרן. פוטנציאלים מקומיים ומדורגים במובן של פוטנציאל מעורר ובכך מפסמים את הממברנה הפוסט-סינפטית של העצב.
כאשר פוטנציאל הממברנה נגזר תוך תאית, הפוטנציאל הפוסט-סינפטי המעורר הוא קיטוב של קרום הסומה. דפולריזציה זו מתרחשת כתוצאה מהתפשטות פסיבית. יש סיכום של פוטנציאלים פרטניים. כמות העצבים המועברים ומשוחררים וגודל פוטנציאל הממברנה השולט קובעים את מידת הפוטנציאל הפוסט-סינפטי המעורר. ככל שהקדם-קיטוב של הממברנה גבוה יותר, כך הפוטנציאל הפוסט-סינפטי המעורר נמוך יותר.
אם הממברנה כבר מפולחת מעל פוטנציאל המנוחה שלה, אז הפוטנציאל לעורר פוסט-סינפטי צונח ובנסיבות מסוימות מגיע לאפס. במקרה זה מושג פוטנציאל ההיפוך של הפוטנציאל המעורר. אם יתברר כי הקדם-דפולריזציה גבוהה עוד יותר, נוצר פוטנציאל עם סימן הפוך. לפיכך, לא תמיד יש להשוות את הפוטנציאל המעורר-פוסט-סינפטי עם קיטוב. זה מזיז את הממברנה דווקא לעבר פוטנציאל שיווי משקל מסוים, שלרוב נשאר מתחת לפוטנציאל הממברנה הנחה בהתאמה.
עבודתו של מנגנון יון מורכב ממלאת תפקיד בכך. עם הפוטנציאל המעורר פוסט-סינפטי, ניתן לראות חדירות קרום מוגברת ליוני אשלגן ונתרן. מצד שני, יכולים להופיע גם פוטנציאלים עם מוליכות נמוכה עבור יוני נתרן ואשלגן. בהקשר זה, ככל הנראה, מנגנון ערוץ היונים הוא הטריגר לסגירת כל תעלות האשלגן הדולפות.
הפוטנציאל הפוסט-סינפטי המעכב הוא ההפך מהפוטנציאל הפוסט-סינפטי המעורר. גם כאן פוטנציאל הממברנה משתנה באופן מקומי בממברנה הפוסט-סינפטית של תאי העצב. היפרפולריזציה של קרום התא מתרחשת בסינפסה, אשר מעכבת את הפעלת פוטנציאל הפעולה במסגרת הפוטנציאל הפוסט-סינפטי המעורר. המעבירים העצביים בסינפסות המעכבות מעוררים תגובה של התא. תעלות הממברנה הפוסט-סינפטית נפתחות ומאפשרות ליוני אשלגן או כלוריד לעבור. יצוא אשלגן יון וזרם יונים של כלוריד גורמים להיפר קיטוב מקומי בקרום הפוסט-סינפטי.
אתה יכול למצוא את התרופות שלך כאן
תרופות לחולשת שריריםמחלות ומחלות
מחלות שונות משבשות את התקשורת בין סינפסות אינדיבידואליות וכך גם הולכת האות בסינפסה הכימית. דוגמא אחת היא המחלה העצבית-שרירית מיאסטניה גרביס, המשפיעה על לוח השריר. זוהי מחלה אוטואימונית מסיבה שלא הייתה ידועה בעבר. במקרה של המחלה, הגוף יוצר נוגדנים אוטומטיים כנגד הרקמה של הגוף עצמו. במחלות שרירים, נוגדנים אלו מכוונים נגד הממברנה הפוסט-סינפטית על גבי לוחות עצב עצביים. לרוב הנוגדנים האוטומטיים במחלה זו הם נוגדנים לקולטן אצטיל כולין. הם תוקפים את קולטני האצטילכולין הניקוטין בנקודות החיבור בין העצבים לשרירים. הדלקת החיסונית המתקבלת הורסת את הרקמה המקומית.
כתוצאה מכך, התקשורת בין עצב לשריר מופר, שכן האינטראקציה בין אצטילכולין לקולטן שלו מתקשה ואף מונעת על ידי נוגדני הקולטן לאצטילכולין. לפיכך, פוטנציאל הפעולה אינו יכול לעבור עוד מהעצב לשריר. לפיכך השריר כבר לא נרגש.
הסכום של כל הקולטנים לאצטילכולין מצטמצם במקביל להרס הקולטנים על ידי הפעילות החיסונית. הממברנות התת-סינפיות מתפרקות ואנדוציטוזיס יוצר אוטופגוזום. שלפוחית הובלה מתמזגת עם האוטופגומים והקולטנים לאצטילכולין משתנים כתוצאה מתגובה חיסונית זו. עם שינויים אלה, כל צלחת הקצה המנועית משתנה. הפער הסינפטי מתרחב. מסיבה זו, אצטילכולין מתפזר מהשסע הסינפטי או מנוטרל מבלי להיקשר לקולטן.
מיסטניות אחרות מראות השפעות דומות על השסע הסינפטי ועל הפוטנציאל הפוסט-סינפטי המעורר.





.jpg)





.jpg)